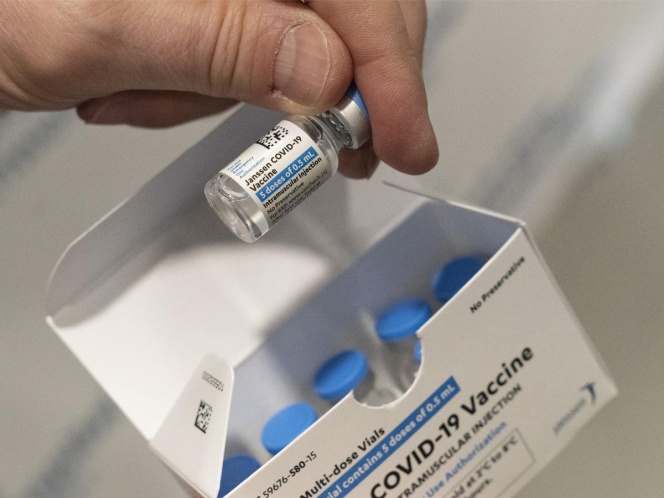
NUEVA YORK. – Una planta que produce las vacunas covid de Johnson & Johnson debe corregir una larga lista de problemas, incluidos pintura descascarada, mala higiene y sustancias marrones y negras en las superficies, dijo la Administración de Drogas y Alimentos de Estados Unidos en un informe de 12 páginas sobre la instalación, que ha detenido la elaboración.
Emergent Biosolutions, con sede en Baltimore, ha buscado la autorización de los reguladores para fabricar la vacuna de J&J allí.
La compañía detuvo la producción en la planta recientemente, diciendo que la FDA se lo solicitó después de una inspección.
Johnson & Johnson reiteró el miércoles que estaba trabajando para establecer una cadena de suministro global en la que 10 sitios de producción estarían involucrados en la elaboración de su vacuna covid-19, además de su planta en Leiden, Holanda.
La FDA dijo que sus inspecciones estaban completas y la agencia emitió un informe que detallaba una larga lista de problemas que se debían remediar, incluida la falta de capacitación del personal para evitar la contaminación cruzada de las vacunas covid-19 de Johnson & Johnson y AstraZeneca, que también se habían producido en el sitio.
Emergent no estuvo disponible de inmediato para hacer comentarios.
La producción de la vacuna AstraZeneca, que aún no está autorizada para su uso en los Estados Unidos, se detuvo previamente en la planta Emergent después de que los ingredientes de esa inyección contaminaron un lote de la vacuna J&J, arruinando millones de dosis.
La FDA también señaló que Emergent no produjo informes adecuados que demuestren que la vacuna que estaba produciendo cumplía con los estándares de calidad.
Sede problemática
La inspección, realizada entre el 12 y el 20 de abril, encontró que el edificio no tenía el tamaño ni el diseño adecuados para facilitar la limpieza, el mantenimiento o las operaciones adecuadas.
Describió que una pared tenía una sustancia marrón.
La FDA también dijo que el equipo utilizado no era del tamaño correcto para una limpieza y mantenimiento adecuados.
El informe de la FDA citó imágenes de cámaras de seguridad del personal de producción llevando bolsas sin sellar de desechos médicos alrededor de la instalación, poniéndolas en contacto con contenedores de material utilizado en la fabricación.
Los empleados tampoco guardaron registro sistemático de las duchas y retiro de batas necesarios al entrar y salir del espacio de fabricación estéril.
J&J dijo que ejercerá su autoridad de supervisión para garantizar que todas las observaciones del regulador se aborden de manera rápida y completa.
Con información de Reuters